Polimerizzazione
merqury2023-02-06T11:27:27+01:00Polimerizzazione significato:
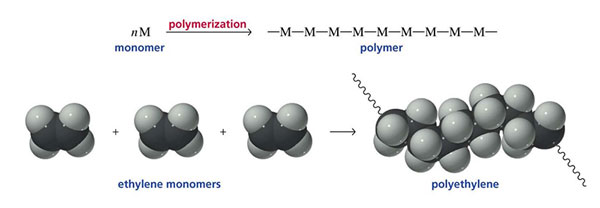
La polimerizzazione è il processo in cui avviene la trasformazione di molecole semplici, o monomeri, in una molecola complessa di grandi dimensioni, detta macromolecola o polimero, avente proprietà chimiche e fisiche molto diverse dalle molecole iniziali.
Polimero
Un polimero è una macromolecola costituito dal ripetersi di un’unità strutturale (unità ripetitiva) di base che deriva da una molecola più piccola e definita detta monomero.
Queste catene polimeriche possono essere formate da poche, migliaia o anche milioni di monomeri legati tramite legame covalente.
Monenclatura
Il gran numero esistente di polimeri naturali o preparati a scopo industriale ha reso necessaria una speciale nomenclatura, che si differenzia da quella usata per i normali composti chimici.
La IUPAC (International Union Pure Applied Chemistry) nel 1952 ha suggerito alcuni criteri che però a tutt’oggi non sono stati unificati; in ogni caso il nome inizia sempre con il prefisso poli-, seguito dal nome che ricorda l’unità base: per esempio polietilene, polifenolo, ecc.
Un altro criterio suggerito, che però non si è molto diffuso, si riferisce al gruppo funzionale del composto chimico che ha reso possibile la polimerizzazione (per esempio polialdeidi, poliammidi, ecc.).
Grado di polimerizzazione
Il numero di unità ripetitive per ogni catena polimerica definisce il grado di polimerizzazione. I polimeri di sintesi sono costituiti da una distribuzione più o meno ampia di catene polimeriche a diverso grado di polimerizzazione.
Perché è importante saperlo?
Perché ne definisce varie caratteristiche fisiche in particolare l’elasticità o il suo reciproco la durezza, le caratteristiche tensili e di resistenza al taglio del Polimero. Piu’ e’ lunga la molecola tanto piu’ questo influenza le caratteristiche del polimero, Un eventuale filo di polimero di carbonio monoatomico avrebbe una resistenza alla trazione tale da sollevare una nave.
Definisce inoltre l’uniformità nel tempo di tali caratteristiche fisiche polimeri molto elastici come ad esempio le gomme sintetiche o i Siliconi sono polimeri relativamente corti con tempi di reticolazione completa di anni.
Metodiche di polimerizzazione
I polimeri di addizione sono quelle macromolecole nelle quali la formula chimica dell’unità ripetente è identica a quella del monomero utilizzato.
I polimeri di condensazione sono composti in cui la formula chimica dell’unità ripetente contiene un numero di atomi inferiore a quello del monomero, o dei monomeri di partenza. La classificazione dei prodotti di polimerizzazione in polimeri di poliaddizione e polimeri di policondensazione fu proposta da Carothers nel 1926.
Una classificazione più recente è fondata invece sul meccanismo di crescita delle macromolecole e distingue i processi di polimerizzazione in polimerizzazione a catena ed in polimerizzazione a stadi.
Le polimerizzazioni a catena si svolgono con un meccanismo del tutto simile alle reazioni a catena tipiche delle sostanze a basso peso molecolare, con l’unica peculiarità che la catena cinetica é in questo caso costituita dalla molecola del polimero che si sta formando.
Si tratta in genere di reazioni veloci che procedono attraverso la formazione di un centro attivo su cui avvengono le successive addizioni ripetute di monomero nel corso della fase di propagazione della catena.
Le polimerizzazioni a stadi sono invece processi nei quali sono coinvolti in genere monomeri opportunamente funzionalizzati che reagiscono dando luogo a prodotti di peso molecolare crescente, che possedendo i medesimi gruppi funzionali presenti sulle molecole di monomero di partenza, nel decorso della reazione possono determinare con uguale probabilità sia interazioni monomero-monomero che interazioni monomero-polimero.
Questa classificazione consente di raggruppare opportunamente tutte le reazioni di polimerizzazione conosciute e di meglio classificarne i rispettivi prodotti.
Pertanto presenteremo le due più grandi famiglie di metodiche di polimerizzazione attuali e cioè POLIMERIZZAZIONE A CATENA e la POLIMERIZZAZIONE A STADI.
1. Polimerizzazione a catena
La polimerizzazione a catena avviene per addizioni successive, e in genere non sono presenti sottoprodotti, quindi, si tratta in genere di una polimerizzazione per addizione.

Questo tipo di polimerizzazione è detto a catena perché ogni passaggio dipende da quello precedente, e permette quello successivo.
In questo genere di reazioni sono coinvolti per lo più monomeri vinilici, ovvero monomeri in cui è presente un doppio legame C=C; sono tuttavia possibili polimerizzazioni a catena anche con monomeri di altro tipo (come ad esempio gli eteri ciclici).
Si possono avere diverse tipologie di polimerizzazione a catena, a seconda della tipologia della specie attiva:
1. POLIMERIZZAZIONE RADICALICA
2. POLIMERIZZAZIONE IONICA
• CATIONICA
• ANIONICA
Nella polimerizzazione radicalica (detta anche poliaddizione radicalica) le molecole reattive sono dei radicali, mentre nelle polimerizzazioni ioniche le molecole reattive sono rispettivamente dei carbocationi e carbanioni. Si differenziano per la modalità di scissione del legame.
Polimerizzazione radicalica
Una delle reazioni più diffuse ed efficenti per ottenere i polimeri è la polimerizzazione radicalica. Viene utilizzata per ottenere polimeri molecole contenenti doppi legami carbonio-carbonio.
In presenza di minime quantità di iniziatore radicalico, molti alcheni a basso peso molecolare subiscono una rapida polimerizzazione.
Ad esempio il polietilene, prodotto industrialmente fin dal 1943, viene sintetizzato ad alta temperatura (180-250°C), ad alta pressione (2000-3000 atm) e in presenza di un catalizzatore radicalico come il perossido di benzoile.
Come tutte le reazioni radicaliche, la polimerizzazione avviene in tre stadi:
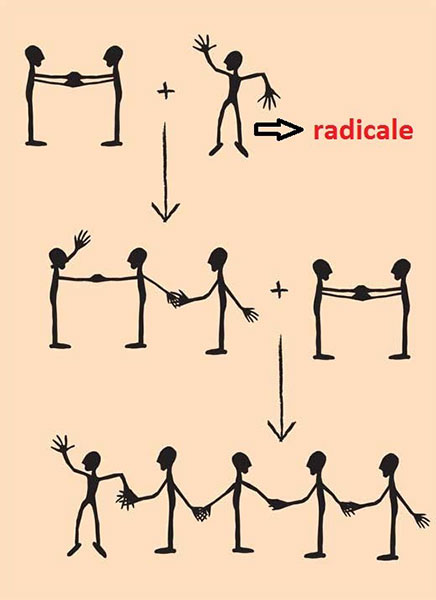
• Inizio: avviene in presenza di tracce di radicali derivanti dal catalizzatore.
• Propagazione: uno dei radicali benzoilossi genera un radicale carbonioso su una molecola di etilene che si addiziona
• Termine: la catena polimerica si arresta quando i radicali vengono consumati per combinazione o per dismutazione.
Polimerizzazione ionica
(CATIONICA E ANIONICA)
Anche questo tipo di polimerizzazioni hanno meccanismo a catena, ma la velocità di polimerizzazione è maggiore di quella radicalica.
Questo poiché in quelle radicaliche si deve generare l’iniziatore (reazione lenta), e quando parte la polimerizzazione non tutti i radicali sono attivi.
Invece in quelle ioniche gli ioni appena introdotti sono subito tutti attivi (questo perché di solito si tratta di acidi forti completamente dissociati).
Quindi l’iniziatore forma immediatamente ed al 100% la specie attiva. Inoltre queste polimerizzazioni presentano stereospecificità elevata e dipendente dal solvente.
La specie propagante è accompagnata da un controione di carica opposta, più o meno separato a seconda del solvente.
Infine non è possibile avere la terminazione per accoppiamento poiché le specie che propagano portano carica dello stesso segno.

2. Polimerizzazione a stadi
Nel meccanismo a stadi è possibile un solo tipo di reazione e può interessare due unità monomeriche, un monomero e un’unità terminale di un polimero o le due unità terminali di due catene polimeriche.
La velocità di reazione di ogni atto è sempre la stessa , ovvero la velocità di reazione tra due monomeri è uguale a quella tra un polimero e un monomero o fra due polimeri.
Questo fatto porta a una certa omogeneità dei pesi molecolari e limita la formazione di catene a elevato peso molecolare, infatti la velocità di reazione risulta proporzionale al numero di gruppi funzionali attivi presenti.
Quando ha luogo un atto di reazione due gruppi funzionali scompaiono e con il procedere della reazione il loro numero si riduce notevolmente con conseguente diminuzione della velocità di polimerizzazione.
Paul Flory verificò sperimentalmente che in alcune reazioni di esterificazione vi era indipendenza della reattività dei gruppi funzionali dalla lunghezza della catena polimerica.
Ne deriva che tutti i gruppi funzionali presenti possono reagire in modo casuale mediante un processo bimolecolare.
Vi sono molte tipologie di polimerizzazione a stadi ma tra le più conosciute ed usate troviamo:
Polimerizzazione per condensazione
Un altro importante meccanismo di polimerizzazione è la polimerizzazione per condensazione.
A differenza dalla polimerizzazione a catena i meccanismi reattivi alla base della policondensazione sono i più svariati della chimica organica.
Possiamo in questa sede citare alcuni esempi più significativi, senza avere la pretesa di essere esaurienti.
Di solito, ma non sempre, una molecola piccola (frequentemente acqua) viene eliminata, mentre ogni unità di monomero viene attaccata al polimero in crescita.
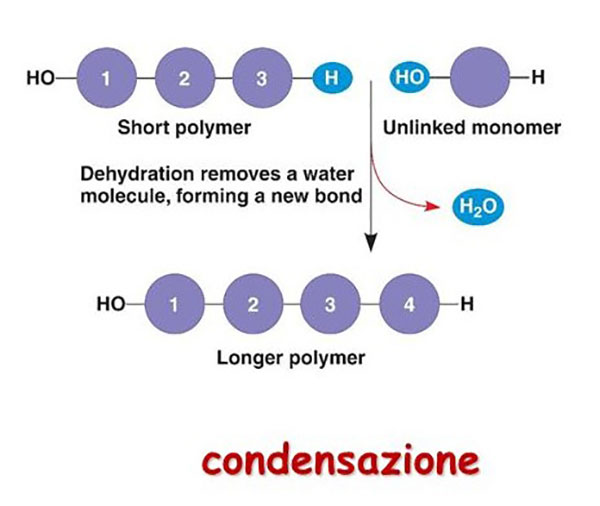
Condizione necessaria perché una determinata sostanza possa partecipare ad una reazione di policondensazione è che il prodotto della prima reazione possa dar luogo ad un’ulteriore reazione dello stesso tipo e cio si possa ripetere per un gran numero di volte.
Questo è possibile quando le molecole dei monomeri contengono almeno due gruppi funzionali idonei, cioè reattivi. Con monomeri bifunzionali si ha policondensazione che porta esclusivamente alla formazione di polimeri lineari come ad esempio Poliammidi. Ad esempio la polimerizzazione dell’acido 6-amminoesanoico.
Le prime due molecole reagiscono al riscaldamento secondo la reazione:
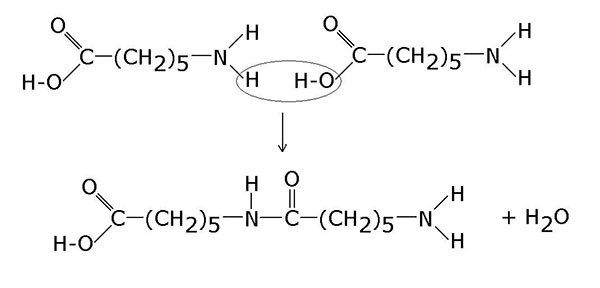
Un’ammina ed un acido carbossilico reagendo danno un legame ammidico ed acqua.
La nuova molecola ha ancora un gruppo amminico ad un terminale ed un gruppo carbossilico acido all’altro terminale; pertanto può reagire con altre due molecole di acido 6 ammino esanoico. Il processo si ripete per costruire una molecola a lunga catena.
Per ogni unità di monomero aggiunta si separa una molecola di acqua. Il polimero finale in questo caso viene chiamato nylon 6 e viene usato nei pneumatici radiali cinturati in fibra e come materiale per ingranaggi autolubrificanti.
Processi di polimerizzazione
Secondo le proprietà dei monomeri di partenza, del meccanismo di reazione, delle necessità applicative sono stati messi a punto numerosi processi di polimerizzazione. ma ne prenderemo in considerazione solo due ovvero: Polimerizzazione in massa.
E’ un processo di conversione diretta di uno o più monomeri nel corrispondente polimero; se il polimero è solubile nel monomero si è in presenza di una fase omogenea durante tutto il corso della polimerizzazione.
I processi commercialmente più importanti sono quelli che avvengono in fase liquida. La possibilità di realizzare industrialmente la polimerizzazione in massa dipende dal calore di polimerizzazione del monomero infatti il processo è applicabile vantaggiosamente quando il valore del calore di polimerizzazione non risulta particolarmente elevato e quindi la reazione risulta facilmente controllabile.
Vi sono inoltre altri fattori che condizionano il successo di tale polimerizzazione quali la reattività del monomero, la conducibilità termica del monomero e del polimero e la viscosità del sistema.
Un monomero troppo reattivo quale l’acrilato di metile, l’acido acrilico, il tetrafluoroetilene, ad esempio, non dà garanzia di un controllo della reazione.
La conducibilità termica inoltre influisce direttamente sulla possibilità di smaltimento del calore di reazione e la viscosità del sistema deve risultare relativamente bassa durante il corso della reazione al fine di avere una facile agitazione e una rapida eliminazione di eventuali prodotti gassosi dall’interno della massa fusa.
La polimerizzazione in massa è utilizzata preferibilmente nei processi che decorrono a stadi ovvero in quelli di policondensazione. Infatti, in tale caso i pesi molecolari crescono gradualmente nel corso della reazione e gli alti pesi molecolari si ottengono solo verso la fine della reazione.
La polimerizzazione in massa è di più difficile applicazione se la reazione avviene tramite un meccanismo a catena: in questo caso si ha un forte sviluppo di calore che va rapidamente smaltito e con elevate viscosità dei prodotti finali che favoriscono fenomeni di surriscaldamento locale.
Il controllo del processo risulta pertanto difficile e si può arrivare finanche a processi di degradazione. Per limitare questo tipo di problematiche è conveniente arrestare il processo a bassi valori di conversione, allontanare il monomero in eccesso e completare la reazione in un secondo stadio.
Esempi di applicazione industriale di polimerizzazione in massa sono:
• La produzione di poliesametilendiammide a partire da esametilendiammina e acido adipico a 200°C e 15 atm fino all’80% di conversione e successivo completamento della reazione a circa 300°C (fibre di nylon)
• La sintesi di polietilentereftalato a partire da glicol etilenico e dimetiltereftalato dalla cui reazione si ottiene il monomero di partenza il bis-2-idrossietiltereftalato (fibre poliestere)
• La sintesi del polistirolo realizzata in due stadi: nel primo a 80°C viene preparato un prepolimero costituito da una soluzione contenente circa il 30% di polimero in stirene che consente ancora un efficiente mescolamento e un buon trasferimento di calore
• La produzione di pezzi di polimetilmetacrilato per polimerizzazione a 60-100 °C di un prepolimero di adatta viscosità colato in opportuni stampi (plexiglass).
Polimerizzazione in soluzione
Il processo avviene in un solvente in cui sia monomero che polimero sono solubili: si realizza così una fase omogenea durante tutto il corso della reazione.
La diluizione evita gli inconvenienti della polimerizzazione in massa per quanto attiene la dissipazione del calore di reazione e realizza condizioni di viscosità compatibili con una facile agitazione della massa.
Permette inoltre di usare più alte temperature di reazione; contemporaneamente, però, la diluizione provoca un rallentamento della velocità di polimerizzazione.
Particolare attenzione deve essere riservata alla scelta del solvente: è molto difficile, infatti, avere a disposizione un solvente inerte che non partecipa in alcun modo alla reazione.
I solventi possono indurre la decomposizione dei catalizzatori: i perossidi sono decomposti da idrocarburi aromatici, alcoli, fenoli, eteri e ammine; possono dar luogo a trasferimento di catena giacché il radicale in crescita può estrarre un atomo di idrogeno dalla molecola di solvente limitando il peso molecolare del polimero che si forma, e facendo iniziare la crescita di un’altra macromolecola dal radicale libero formatosi dal solvente.
Quanto più estesa è questa azione e tanto più basso sarà il peso molecolare medio del polimero finale.
Per avere un polimero puro è, inoltre, necessario allontanare completamente il solvente alla fine della reazione. Questa operazione può risultare a volte piuttosto difficile.
Quindi la polimerizzazione in soluzione sarà applicata di preferenza quando il polimero potrà essere usato in soluzione per applicazioni tipo vernici e adesivi .
Esempi di grande importanza industriale sono il processo Phillips per la produzione a bassa pressione di polietilene ad alta densità, in idrocarburi alifatici, in presenza di ossido di cromo su adatti substrati come silicati di alluminio e il processo Standard Oil che utilizza come catalizzatore un ossido di metalli di transizione del V o VI gruppo su un supporto poroso come ossido di molibdeno su allumina.
Altri esempi sono la preparazione di copolimeri stirene- anidride maleica in benzene o in acetone, la reazione di reticolazione con stirene di resine alchiliche insature, la produzione di polivinilacetato in acetato di etile, la produzione di acido poliacrilico, di poliacrilammidi e di polivinilpirrolidone in acqua.












